كان أوائل القرن العشرين وقتًا ميمونًا جدًا للعلوم. بالإضافة إلى إرنست رذرفورد ونيلز بور ، اللذين ولدا النموذج القياسي لفيزياء الجسيمات ، كانت أيضًا فترة من الاختراقات في مجال ميكانيكا الكم. بفضل الدراسات الجارية حول سلوك الإلكترونات ، بدأ العلماء في اقتراح نظريات تتصرف بها هذه الجسيمات الأولية بطرق تتحدى فيزياء نيوتن الكلاسيكية.
أحد الأمثلة على ذلك هو نموذج السحابة الإلكترونية الذي اقترحه Erwin Schrodinger. بفضل هذا النموذج ، لم يعد يتم تصوير الإلكترونات على أنها جسيمات تتحرك حول نواة مركزية في مدار ثابت. وبدلاً من ذلك ، اقترح شرودنغر نموذجًا يمكن للعلماء من خلاله إجراء تخمينات مدروسة فقط فيما يتعلق بمواقع الإلكترونات. وبالتالي ، لا يمكن وصف مواقعها إلا على أنها جزء من "سحابة" حول النواة حيث من المحتمل أن يتم العثور على الإلكترونات.
الفيزياء الذرية حتى القرن العشرين:
تأتي أقدم الأمثلة المعروفة للنظرية الذرية من اليونان والهند القديمة ، حيث افترض فلاسفة مثل ديموقريطس أن كل المادة تتكون من وحدات صغيرة غير قابلة للتجزئة وغير قابلة للتدمير. صُمم مصطلح "الذرة" في اليونان القديمة وأدى إلى ظهور مدرسة الفكر المعروفة باسم "الذرة". ومع ذلك ، كانت هذه النظرية مفهومًا فلسفيًا أكثر من كونها علمية.
لم يتم حتى القرن التاسع عشر أن تُفصَّل نظرية الذرات كمسألة علمية ، مع إجراء التجارب الأولى المستندة إلى الأدلة. على سبيل المثال ، في أوائل القرن التاسع عشر الميلادي ، استخدم العالم الإنجليزي جون دالتون مفهوم الذرة لشرح سبب تفاعل العناصر الكيميائية بطرق معينة يمكن ملاحظتها ويمكن التنبؤ بها. من خلال سلسلة من التجارب التي تنطوي على الغازات ، ذهب دالتون لتطوير ما يعرف بالنظرية الذرية لدالتون.
توسعت هذه النظرية في قوانين المحادثة ذات النسب الجماعية والقصيرة ونزلت إلى خمسة أسس: العناصر ، في أنقى حالاتها ، تتكون من جزيئات تسمى الذرات ؛ ذرات عنصر معين هي نفسها ، حتى آخر ذرة ؛ يمكن التمييز بين ذرات العناصر المختلفة من خلال أوزانها الذرية ؛ تتحد ذرات العناصر لتكوين مركبات كيميائية ؛ لا يمكن إنشاء أو تدمير الذرات في التفاعل الكيميائي ، بل يتغير التجميع دائمًا.
اكتشاف الإلكترون:
بحلول أواخر القرن التاسع عشر ، بدأ العلماء أيضًا في التفكير في أن الذرة تتكون من أكثر من وحدة أساسية واحدة. ومع ذلك ، غامر معظم العلماء بأن هذه الوحدة ستكون بحجم أصغر ذرة معروفة - الهيدروجين. بحلول نهاية القرن التاسع عشر ، سيتغير بشكل جذري ، بفضل البحث الذي أجراه علماء مثل السير جوزيف جون طومسون.
من خلال سلسلة من التجارب باستخدام أنابيب أشعة الكاثود (المعروفة باسم أنبوب كروكس) ، لاحظ طومسون أن أشعة الكاثود يمكن أن تنحرف عن طريق المجالات الكهربائية والمغناطيسية. وخلص إلى أنه بدلاً من كونها مكونة من ضوء ، فإنها تتكون من جزيئات مشحونة بالسالب أصغر مرة واحدة وأخف بمقدار 1800 مرة من الهيدروجين.

هذا دحض بشكل فعال فكرة أن ذرة الهيدروجين كانت أصغر وحدة للمادة ، وذهب طومسون أبعد من ذلك ليقترح أن الذرات قابلة للقسمة. لشرح الشحنة الإجمالية للذرة ، والتي تتكون من كل من الشحنات الإيجابية والسلبية ، اقترح طومسون نموذجًا يتم بموجبه توزيع "الكريات" ذات الشحنة السالبة في بحر موحد من الشحنة الموجبة - المعروف باسم نموذج البرقوق.
سميت هذه الجسيمات لاحقًا باسم "الإلكترونات" ، استنادًا إلى الجسيم النظري الذي تنبأ به الفيزيائي الأنجلو أيرلندي جورج جونستون ستوني في عام 1874. ومن هذا ، ولد نموذج البرقوق ، سميت بذلك لأنها تشبه الصحراء الإنجليزية التي تتكون من كعكة البرقوق والزبيب. تم تقديم المفهوم إلى العالم في إصدار مارس 1904 من المملكة المتحدة مجلة فلسفية ، الى اشادة واسعة.
تطوير النموذج القياسي:
كشفت التجارب اللاحقة عن عدد من المشكلات العلمية في نموذج حلوى البرقوق. بالنسبة للمبتدئين ، كانت هناك مشكلة في إثبات أن الذرة تمتلك شحنة خلفية إيجابية موحدة ، والتي أصبحت تعرف باسم "مشكلة طومسون". بعد خمس سنوات ، سيتم دحض النموذج من قبل هانز جايجر وإرنست مارسدن ، الذين أجروا سلسلة من التجارب باستخدام جسيمات ألفا وورق الذهب - المعروف أيضًا. تجربة "رقائق الذهب".
في هذه التجربة ، قام Geiger و Marsden بقياس نمط تشتت جسيمات ألفا مع شاشة الفلورسنت. إذا كان نموذج طومسون صحيحًا ، فستمر جسيمات ألفا من خلال التركيب الذري للرقاقة بدون عوائق. ومع ذلك ، لاحظوا بدلاً من ذلك أنه في حين أن معظمهم يتم إطلاق النار من خلاله مباشرة ، فإن بعضهم مشتتون في اتجاهات مختلفة ، مع عودة البعض الآخر باتجاه المصدر.

استنتج Geiger و Marsden أن الجسيمات واجهت قوة إلكتروستاتيكية أكبر بكثير من تلك التي سمح بها نموذج طومسون. بما أن جزيئات ألفا هي مجرد نوى هيليوم (مشحونة بشكل إيجابي) ، فهذا يعني أن الشحنة الموجبة في الذرة لم تنتشر على نطاق واسع ، ولكنها تتركز في حجم صغير. بالإضافة إلى ذلك ، حقيقة أن تلك الجسيمات التي لم تنحرف تمر عبر عوائق تعني أن هذه المساحات الإيجابية تم فصلها بواسطة فجوات واسعة من الفضاء الفارغ.
بحلول عام 1911 ، قام الفيزيائي إرنست رذرفورد بتفسير تجارب جيجر مارسدن ورفض نموذج طومسون للذرة. وبدلاً من ذلك ، اقترح نموذجًا تتكون فيه الذرة من مساحة فارغة في الغالب ، مع تركيز كل شحنتها الإيجابية في مركزها في حجم صغير جدًا ، محاطًا بسحابة من الإلكترونات. أصبح هذا يعرف باسم نموذج روثرفورد للذرة.
صقلت التجارب اللاحقة التي قام بها أنطونيوس فان دن برويك ونيلز بور النموذج أكثر. في حين اقترح فان دن برويك أن العدد الذري لعنصر مشابه جدًا لشحنته النووية ، فقد اقترح الأخير نموذجًا يشبه النظام الشمسي للذرة ، حيث تحتوي النواة على العدد الذري للشحنة الموجبة ويحيط بها متساوي عدد الإلكترونات في الأصداف المدارية (المعروفة أيضًا بنموذج بور).
نموذج سحابة الإلكترون:
خلال عشرينيات القرن العشرين ، أصبح الفيزيائي النمساوي إروين شرودنغر مفتونًا بالنظريات ماكس بلانك ، ألبرت أينشتاين ، نيلز بور ، أرنولد سومرفيلد ، وغيرهم من الفيزيائيين. خلال هذا الوقت ، شارك أيضًا في مجالات النظرية الذرية والأطياف ، وأجرى أبحاثًا في جامعة زيورخ ثم جامعة فريدريش فيلهلم في برلين (حيث خلف بلانك في عام 1927).

في عام 1926 ، تناول شرودنغر قضية الدالات الموجية والإلكترونات في سلسلة من الأوراق. بالإضافة إلى وصف ما سيُعرف باسم معادلة شرودنغر - معادلة تفاضلية جزئية تصف كيف تتغير الحالة الكمية لنظام كمومي مع الوقت - استخدم أيضًا معادلات رياضية لوصف احتمالية العثور على إلكترون في موضع معين .
أصبح هذا أساس ما سيعرف باسم نموذج سحابة الإلكترون (أو ميكانيكا الكم) ، بالإضافة إلى معادلة شرودنغر. بناءً على نظرية الكم ، التي تنص على أن كل المادة لها خصائص مرتبطة بوظيفة الموجة ، يختلف نموذج السحابة الإلكترونية عن نموذج بوهر في أنه لا يحدد المسار الدقيق للإلكترون.
بدلاً من ذلك ، يتنبأ بالموقع المحتمل لموقع الإلكترون بناءً على دالة الاحتمالات. تصف دالة الاحتمالات أساسًا منطقة تشبه السحابة يُرجح وجود الإلكترون فيها ، ومن هنا جاء الاسم. حيث تكون السحابة أكثر كثافة ، يكون احتمال العثور على الإلكترون أكبر. وحيث تقل احتمالية وجود الإلكترون ، تكون السحابة أقل كثافة.
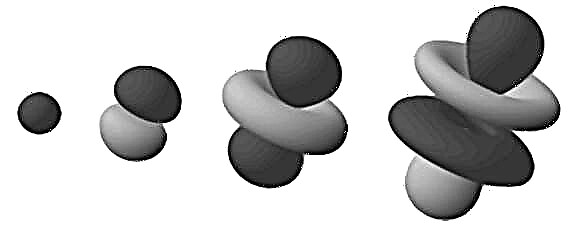
تُعرف هذه المناطق الكثيفة باسم "مدارات الإلكترون" ، نظرًا لأنها الموقع الأكثر ترجيحًا حيث يوجد إلكترون مدار. من خلال توسيع نموذج "السحابة" هذا إلى مساحة ثلاثية الأبعاد ، نرى ذرة حديدية أو ذرة على شكل زهرة (كما في الصورة في الأعلى). هنا ، المناطق المتفرعة هي تلك التي من المرجح أن نجد فيها الإلكترونات.
بفضل عمل شرودنغر ، بدأ العلماء في فهم أنه في عالم ميكانيكا الكم ، كان من المستحيل معرفة الموقع الدقيق وزخم الإلكترون في نفس الوقت. بغض النظر عما يعرفه المراقب في البداية عن الجسيم ، يمكنهم فقط توقع موقعه أو زخمه التالي من حيث الاحتمالات.
ولن يتمكنوا في أي وقت من التحقق من أي منهما. في الواقع ، كلما عرفوا أكثر عن زخم الجسيم ، قل معرفتهم بموقعه ، والعكس صحيح. هذا ما يعرف اليوم باسم "مبدأ عدم اليقين".
لاحظ أن المدارات المذكورة في الفقرة السابقة تتكون من ذرة هيدروجين (أي بإلكترون واحد فقط). عند التعامل مع الذرات التي تحتوي على المزيد من الإلكترونات ، تنتشر المناطق المدارية الإلكترونية بالتساوي في كرة ضبابية كروية. هذا هو المكان الأكثر ملاءمة لمصطلح "سحابة الإلكترون".
تم الاعتراف بهذه المساهمة على نطاق عالمي باعتبارها واحدة من المساهمات الهامة من حيث التكلفة في القرن العشرين ، والتي أطلقت ثورة في مجالات الفيزياء وميكانيكا الكم وفي الواقع جميع العلوم. من الآن فصاعدًا ، لم يعد العلماء يعملون في عالم يتميز بقيم مطلقة للزمان والمكان ، ولكن في حالة عدم اليقين الكمي والنسبية الزمانية!
لقد كتبنا العديد من المقالات المثيرة للاهتمام حول الذرات والنماذج الذرية هنا في مجلة الفضاء. إليكم ما هو النموذج الذري لجون دالتون ؟، ما هو نموذج البرقوق ؟، ما هو نموذج بور الذري ؟، من كان ديموقراطي ؟، وما هي أجزاء الذرة؟
لمزيد من المعلومات ، تأكد من التحقق من ما هي ميكانيكا الكم؟ من Live Science.
يلقي فريق علم الفلك أيضًا حلقة حول هذا الموضوع ، مثل الحلقة 130: راديو علم الفلك ، الحلقة 138: ميكانيكا الكم ، والحلقة 252: مبدأ عدم اليقين هايزنبرغ